|
 Notas Notas
Estimulación Vagal en la
Epilepsia: Consideraciones Anestésicas.
Dra. María
Luisa Meilán
Luis
Quecedo Gutierrez
Médicos Adjuntos
Hospital de la
Princesa. Madrid. España.
http://www.uam.es/departamentos/medicina/anesnet/forconred/neuro/vago/vago.htm
Introducción
La epilepsia es una enfermedad crónica con
una incidencia del 1% que altera en gran medida la calidad de vida de los
pacientes afectados. (1) A pesar de los recientes avances tecnológicos en el
diseño de nuevos fármacos, el control de las crisis no es satisfactorio en el
30-40% de los pacientes, siendo alrededor de un 15% los pacientes que obtienen
en mayor o menor grado mejoría tras alguna de las distintas técnicas
quirúrgicas.(2) (3)
Los avances en el conocimiento sobre las
bases anatómicas y patofisiológicas de la epilepsia, ha propiciado el desarrollo
de técnicas complementarias al tratamiento médico-quirúrgico clásico de la
epilepsia refractaria. La neuroestimulación vagal es una técnica antigua pero
aprobada recientemente por la FDA, que se fundamenta en la estimulación
eléctrica intermitente del tronco del nervio vago a nivel cervical
izquierdo.(4). La descripción del procedimiento y sus implicaciones en la
practica anestésica, así como, sus posibles complicaciones cardio-respiratorias
son los objetivos fundamentales de este trabajo.(4).
Anatomía del
Nervio Vago
El nervio vago se compone de: Fibras
motoras viscerales generales (parasimpáticas) y especiales, sensitivas
viscerales generales y especiales, fibras sensitivas somáticas.(5)
-
Las fibras parasimpáticas inervan el
corazón, los pulmones y el tubo digestivo casi hasta el ángulo esplénico del
colon.
-
Las fibras motoras viscerales especiales
inervan los fascículos estriados de la laringe, la faringe y el paladar.
-
Las fibras sensitivas viscerales
generales proceden de la mucosa del paladar, faringe y laringe, así como del
corazón, los pulmones y el tubo digestivo.
-
Las fibras sensitivas viscerales
especiales (gusto) proceden de la valécula y la epiglotis.
-
Las fibras sensitivas somáticas inervan
la parte posterior del conducto auditivo externo y de la membrana timpánica.
|
 |
Los núcleos vagales situados en la
región del bulbo se distribuyen como: dorsales motor y sensitivo
(parasimpático), el núcleo ambiguo (motor visceral especial) y el núcleo del
tracto solitario (sensitivo visceral). Las fibras sensitivas somáticas
probablemente se conectan con el núcleo sensitivo del trigémino. El nervio
sale del bulbo por fuera de la oliva en forma de pequeñas raíces y del
cráneo a través del agujero rasgado posterior, con el seno petroso inferior
y el nervio glosofaringeo medialmente y el nervio espinal y la vena yugular
interna lateralmente. Desciende por el cuello y el tórax hasta el plexo
esofágico en donde se une con el nervio del otro lado para formar los
troncos vagales anterior y posterior. Junto a la base del cráneo el vago
conforma los ganglios sensitivos superior e inferior.
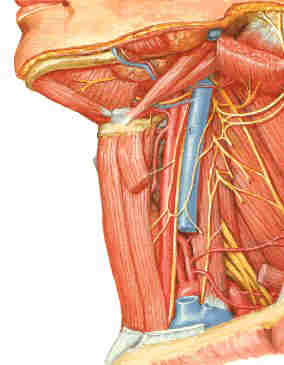
El nervio vago está profundamente
situado en la vaina carotidea (paquete vásculonervioso del cuello), entre la
vena yugular interna (lateralmente) y la arteria carótida (medialmente),
localizándose sobre la aponeurosis y los fascículos prevertebrales. A nivel
de la raíz del cuello, sobre el lado derecho, el nervio discurre anterior a
la arteria subclavia y penetra en el tórax. En el lado izquierdo discurre
entre las arterias carótida común y subclavia para entrar en el tórax. |
RAMAS (en el cuello):
Nervio auricular. Inerva la parte
posterior del conducto auditivo externo y de la membrana timpánica.
Nervios faríngeos. Discurren entre
las arterias carótidas interna y externa hasta llegar al plexo faríngeo e
inervan los fascículos y la mucosa de la faringe y el velo del paladar.
Nervio laríngeo superior.
Desciende entre la faringe (medialmente) y las carótidas interna y externa y se
divide por debajo del hioides en sus ramas superior (interna) e inferior
(externa). La superior perfora la membrana tirohioidea e inerva la mucosa de la
laringe por encima de las cuerdas vocales. El nervio inferior desciende por la
laringe e inerva el fascículo cricotiroideo.
Ramas cardiacas cervicales.
Desciende por ambos lados hasta los plexos cardiacos.
Nervio laríngeo inferior (o recurrente)
derecho. Contornea la arteria subclavia derecha y asciende luego por el
surco entre el esófago y la tráquea. Penetra en la laringe e inerva los
fascículos intrínsecos excepto el cricotiroideo y la mucosa situada por debajo
de las cuerdas vocales.
Fisiopatología y Bases Teóricas
Hace aproximadamente 2000 años Pelops,
maestro de Galeno, sugirió que el estimulo aferente puede modular la actividad
de las crisis epilépticas. Posteriores estudios confirmaron que la estimulación
de las fibras aferentes cutáneas y otras vías sensoriales pueden afectar a los
registros encefalográficos.(6)
En 1938, Bailey y Bremer describen la
representación cortical del nervio vago y registran las alteraciones en la
actividad cerebral después de la estimulación vagal aferente.(7) En la
actualidad se sabe que más del 90% de las fibras vagales son proyecciones
aferentes que se originan en receptores viscerales y terminan en áreas difusas
del sistema nervioso central donde ejercen efectos de neuroexcitabilidad.
Estudios en animales y humanos sugieren que algunas fibras aferentes tienen
conexiones con los núcleos del tracto solitario y así enlazan con el cerebelo,
hipotálamo, amídgdala, hipocampo, formación reticular media, rafé dorsal, locus
ceruleus, núcleo ambiguo, tálamo, cortex insular (4)
El mecanismo por el que el nervio vago
modula la actividad eléctrica cerebral y su lugar de acción es todavía incierto.
El máximo interés se ha centrado en los efectos a nivel del tronco cerebral como
zona epileptógena y reguladora de la propagación de la crisis; así algunos
autores relacionan su acción antiepiléptica con los efectos en el sistema
activador reticular del tronco.(8) (9)
Ben Menachem et al, describen dos posibles
teorías sobre el mecanismo de acción:
-
Eleva el umbral epileptógeno en las
conexiones nerviosas entre el núcleo del tracto solitario y otras
estructuras.(10)
-
Incrementa el número de neurotransmisores
inhibidores y disminuyen los neurotransmisores excitadores. (10)
Agentes inhibidores como el ácido gamma
aminobutírico (GABA), la glicina y otros neurotransmisores, incluyendo: el
glutamato, serotonina, colecistoquinina, neurotensina, angiotensina II,
catecolaminas y opioides endógenos, parecen mediar la transmisión de los
impulsos aferentes vagales. (4)
Se realizaron estudios de metabolitos de
aminoácidos y neurotransmisores en el LCR en 16 pacientes después de 3 meses de
estimulación vagal. Las concentraciones de fosfoetanolamina aumentaron en
pacientes que respondieron y el GABA libre aumentó más en los que no
respondieron. Hubo una correlación significativa entre reducción de las crisis e
incremento de la asparagina, fenilalanina, PEA, alanina y triptófano . La
estimulación crónica vagal parece tener efecto en varios aminoácidos del
cerebro. (11)
Un dato importante a tener en cuenta es la
activación de las vías que controlan las funciones viscerales como la tos,
deglución, vómito, digestión y homeostasis interna. Aunque estas vías están
generalmente mediadas por fibras mielínicas aferentes con velocidades de
conducción superiores a 15 m/seg., Chase et al. demuestran que la intensidad de
la estimulación y las frecuencias que se relacionan con una discreta actividad
de desincronización cortical son vehiculizadas por grupos de fibras que
transmiten de 1 a 15 m/seg. Se especula que los efectos antiepilépticos del vago
derivan de la estimulación diferencial de fibras no mielínicas con baja
velocidad de conducción y diámetros pequeños. Estas fibras no mielínicas
incluyendo las A-delta y fibras C constituyen la gran mayoría del nervio vago.
(4)
La estimulación del nervio vago derecho e izquierdo tienen
igual efecto en el control de las crisis epilépticas de modelos animales . Con
la estimulación bilateral no se consiguen mayores beneficios. Los cambios EEG
inducidos por la estimulación vagal son semejantes en ambos hemicortex. Por el
contrario, la inervación eferente vagal es asimétrica: En el corazón, el nervio
vago derecho inerva el nodo sinoauricular, mientras que el izquierdo lo hace
sobre el nodo aurículoventricular, de ahí que el sistema de estimulación vagal
se inserte en el lado izquierdo.
(9) (12)
Técnica
Quirúrgica
La colocación del primer estimulador vagal
en humanos se realizó en 1988. Desde entonces más de 1000 pacientes han
participado en 7 ensayos clínicos en 26 paises y existe una experiencia en más
de 2000 pacientes. (13) (14) (15). Los ensayos en modelos animales y humanos
parecen demostrar un descenso en la frecuencia, duración e intensidad de las
crisis epilépticas, con reducción en la severidad y duración de la
sintomatología postictal. (16) (17) (18)
Se han obtenido tres tipos de patrones de
respuestas al tratamiento: rápida y sostenida, gradual y ausencia total incluso
después de periodos prolongados de estimulación (15)
|
La técnica quirúrgica no es complicada,
pero precisa que el cirujano esté familiarizado con la anatomía del cuello.
La duración no suele ser superior a las dos horas y se realiza habitualmente
con anestesia general. Aunque se podría incluir dentro de la cartera de
servicios de la cirugía mayor ambulatoria, es recomendable mantener al menos
24 horas de vigilancia en prevención de los posibles efectos secundarios de
la técnica |
 |
Se realizan dos incisiones de entrada: la
primera de 8 cm por debajo de la clavícula destinada a la colocación del
generador de pulsos; la siguiente de 7cm servirá para localizar el nervio vago
del lado izquierdo. Está última discurre a lo largo del borde anterior del
músculo esternocleidomastoideo disecando consecutivamente el platisma colli
superficialis y la fascia cervical profunda. Por palpación del pulso carotideo
se identifica la vaina neurovascular, primero se diseca la vena yugular interna
y a continuación, con ayuda del microscopio, el nervio dejando por lo menos 4cm
de la vaina al descubierto. Se colocan los electrodos helicoidales, que
presentan un diámetro de 2mm y se realiza un ajuste holgado para evitar posibles
compresiones.
|
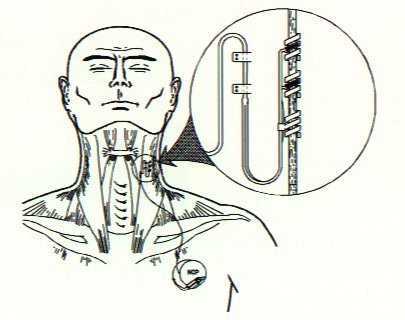 |
Una vez colocados los electrodos se
realiza un test de prueba ( figura adjunta), que consiste en la estimulación
durante un minuto y a una frecuencia de 20Hz, con salida de corriente de 1mA
y pulsos de 500microsg. Durante la estimulación es imprescindible la
monitorización del paciente en prevención de severas bradicardias. Una vez
finalizado el test se deja inactivo el generador durante la primera o
segunda semana del postoperatorio.
Por último, concluida la prueba del test, se inicia el cierre del bolsillo subcutáneo donde va colocado el
generador que se conecta con el electrodo mediante múltiples puntos con la
fascia cervical, a modo de uniones de seguridad. |
INDICACIONES Y
SELECCIÓN DE CRITERIOS
UNIVERSIDAD DE SOUTHERN
CALIFORNIA
|
CRITERIOS DE INCLUSION
|
|
EDAD 12 A 65 AÑOS |
|
CRISIS PARCIALES O 2ª GENERALIZADAS
|
|
IDIOPATICAS O DE ORIGEN ESTRUCTURAL
|
|
PERIODO INTERICTAL <3 SEMANAS
|
|
FALLO
DE LA MEDICACIÓN TRAS 1 MES CON UNA O TRES DROGAS CON
NIVELES ESTABLES |
|
CRITERIOS DE EXCLUSION
|
|
VAGOTOMIA CERVICAL PREVIA
|
|
ENFERMEDAD NEUROLOGICA PROGRESIVA O ENFERMEDAD
SISTEMICA |
|
ARRITMIA CARDIACA |
|
ASMA O EPOC |
|
ULCERA PEPTICA |
|
DIABETES INSULIN DEPENDIENTE
|
|
EMBARAZO |
|
HISTORIA DE CRISIS NO EPILÉPTICA
|
|
IMPOSIBILIDAD DE OBTENER CONSENTIMIENTO
|
|
Técnica Anestésica.
Complicaciones.
La profilaxis antibiótica se
inicia en el preoperatorio y se mantiene durante las primeras 24 h.
del postoperatorio.
La colocación del estimulador
se realiza bajo anestesia general convencional, siendo el periodo
postoperatorio el momento donde la vigilancia debe ser más estrecha
habida cuenta de las posibles complicaciones que produce la
estimulación del nervio vago.
Complicaciones menores:
La mayoría de las
complicaciones menores son benignas y se resuelven solas en las
primeras 24 horas.
|
RONQUERA |
20-66%
|
|
TOS
|
7-45%
|
|
DISNEA
|
6-25%
|
|
CEFALEAS |
14-24%
|
|
NAUSEAS
|
7-15%
|
|
ESPASMO
DEL CUELLO |
11%
|
|
No se han registrado casos de
ulcera gástrica o complicaciones derivadas de un exceso de
secreción gástrica. (18) (19) (20).
Complicaciones
mayores:
|
Asistolia |
Neurology 1999, 12; 52(6): 1267-1269
|
|
Arritmias |
Seizure
1998, 7 (3):213-7 |
|
Muerte
súbita (0,47%) |
Epilepsia, 1998, 39 (2): 206-12
|
|
Estimulación del n. frénico
|
Neurology 1998, 51 (4): 1224-5
|
|
Aspiración |
Epilepsia 1998; 39(9):998-1000
|
|
Alteración
sobre el FSC |
Epilepsia 1998; 39 (9):983-90
|
|
Efectos
sobre la vía aérea |
Epilepsia Res 1994, 18 (2) : 149-54
|
|
Bibliografía
1.- Porter RJ.: Epilepsy:
Prevalence,classification,diagnosis, and prognosis, in Apuzzo MLJ ed:
Neurosurgical Aspects of Epilepsy. Park Ridge, AANS, 1991: 17-26.
2.- NIH Consensus Conference: Surgery for
epilepsy. JAMA 1990; 264: 729-733.
3.- Wilder BJ. Summary and conclusions.
Epilepsia 31[ Suppl 2] : S60,1990).
4.- Amar A P, Heck C N, Levy M L et al.
Neurosurgery 1998, 43: 1265-1280.
5.- Lumley J S P, Craven J L, Aitken J T. Oido,
región intracraneal y nervios craneales. Anatomia esencial.
Aplicaciones técnicas. ed. Barcelona. Salvat. 1985; 333-347.
6.- Rutecki P. Anatomical, physiological, and
theoretical basis for the an tiepileptic effect of vagus nerve
stimulation. Epilepsia 31 [Suppl. 2]: S1-S6,1990.
7.- Bailey P., Bremer F: A sensory cortical
representation of the vagus nerve with a note on the effects of low
blood pressure on the cortical electrogram. J. Neurophysiol 1938; 1:
405-412.
8.- Naritoku DK, Morales A, Pencek TL, Winkler
D: Chronic vagus nerve stimulation increases the latency of the
thalamocortical somatosensory evoked potential. PACE Pacing Clin
Electrophysiol. 1992; 15: 1572-1578.
9.- Vagus Nerve Stimulation Study Group: A
randomized controlled trial of chronic vagus nerve stimulation for
treatment of medically intractable seizures. Neurology. 1995; 45:
224-230.
10.- BenMenachem E. Baillieres Clin Neurol
1996; 5,4: 841-8.
11.- Ben Menachem E. Hamberger A., Hedner T.,
Hammond EJ., Uthman B M et al. Effets of vagus nerve stimulation on
amino acids and other metabolites in the CSF of patients with
partial seizures. Epilepsy Res. 1995, 20,3: 221-7.
12.- Uthman BM, Wilder BJ, Penry JK, Dean C,
Ramsay RE, et al. Treatment of epilepsy by stimulation of the vagus
nerve. Neurology, 1993; 43: 1338-1345.
13.- Landay HJ, Ramsay RE, Slater J, Casiano
RR, Morgan R. Vagus nerve stimulation for complex partial seizures:
surgical technique , safety, and efficacy. J Neurosurg
1993;78:26-31.
14.- Penry JK, Dean JC. Prevention of
intractable partial seizures by intermittent vagal stimulation in
humans: Preliminary results. Epilepsia 1990;31:s40-s43.
15.- Uthman BM, Wilder BJ, Penry JK, Dean C,
Ramsay RE, Reid SA, Hammond EJ, Tarver WB, Wernike JF. Treatment of
epilepsy by stimulation of the vagus nerve. Neurology
1993;43:1338-45.
16.- Murphy JV, Hornig G, Schallert G. Left
vagal nerve stimulation in children with refractory epilepsy.
Preliminary observations. Arch Neurol 1995;52(9):886-9.
17.- Uthman BM, Wilder BJ, Hammond EJ, Reid
SA. Efficacy and safety of vagus nerve stimulation in patients with
complex partial seizures. Epilepsia 1990;31:S44-S50.
18.- Henry TR, Bakay RAE, Votaw JR, Pennell
PB, Epsein CM, Faber TL, Grafton ST, Hoffman JM. Acute vagus nerve
stimulation selectively alters blood flow in somatosensory and
limbic cortex and the cerebellum of patients with complex partial
seizures. Epilepsia 1997;38:144.
19.- Holder LK, Wernicke JF, Tarver WB.
Treatment of refractory partial seizures: Preliminary results of a
controlled study. PACE 1992;15(10 II):1557-71.
20.- Ramsay RE, Uthman BM, Augustinsson LE,
Upton AR, Naritoku D, Willis J, Treig T, Barolat G, Wernicke JF.
Vagus nerve stimulation for treatment of partial seizures: 2. Safety,
side effects, and tolerability. First International Vagus Nerve
Stimulation Study Group. Epilepsia 1994;35(3):627-36.
|