:
– Línea basal. El EEG
basal antes del estímulo puede ser notablemente diferente del EEG basal del
paciente en vigilia, debido al anestésico administrado. A menudo consiste en una
mezcla de actividad rápida y actividad lenta que puede ser de mayor amplitud que
la observada durante la vigilia. El efecto varía dependiendo del grado de
profundidad de la anestesia.
– Estimulación
eléctrica. Durante este período la actividad EEG está bloqueada por la
interferencia de la corriente de estímulo.
– Actividad preictal.
Tras el estímulo eléctrico, puede observarse algunas veces un breve período
preictal de actividad rápida de baja amplitud.
– Ritmo de
reclutamiento epiléptico. Consiste en un período breve de actividad muy rítmica,
de amplitud baja a
moderada en el rango
alfa o beta, que aparece tras la actividad preictal. Se cree que este fenómeno
está asociado a los efectos sincronizantes de las proyecciones talamocorticales
durante las fases tempranas de la generalización de la convulsión.
– Actividad de
polipuntas. Frecuentemente, la fase más temprana que se logra observar en la
convulsión está caracterizada por una actividad de polipuntas de alta
frecuencia. Esta fase coincide con los componentes tónicos
y clónicos tempranos
de la respuesta motora y suele durar entre 10 y 15 s.
– Complejos de
polipuntas y ondas lentas. Durante la fase clónica de la respuesta motora ictal,
la actividad de polipuntas evoluciona a complejos repetitivos de polipuntas y
ondas lentas, que son sincrónicos con los movimientos clónicos y que van
disminuyendo en frecuencia a medida que progresa la fase clónica.
– Fase de
finalización. La amplitud y la regularidad del patrón de polipuntas y ondas
lentas disminuyen gradualmente. En algunos casos, la fase de polipuntas y ondas
lentas puede terminar bruscamente.
|
 |
|
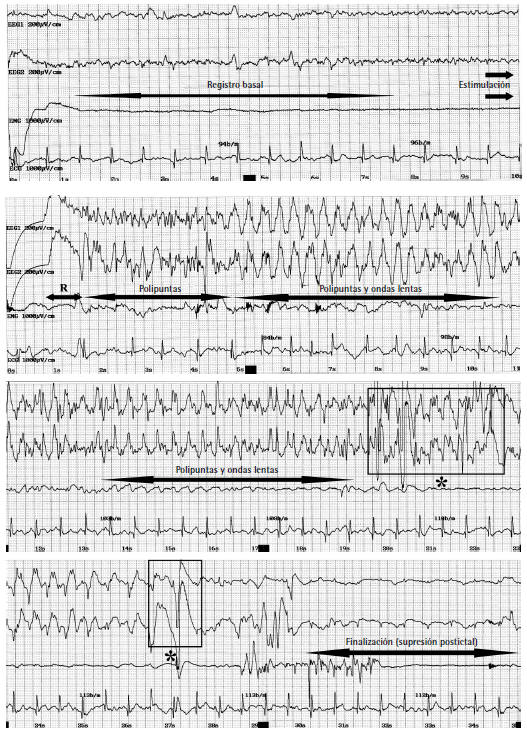
Registro
electroencefalográfico de diferentes fases de la convulsión típica de la
TEC.
EEG:
electroencefalograma; EMG: electromiograma; ECG: electrocardiograma; R:
fase de reclutamiento. Los asteriscos
señalan artefactos
en el registro provocados por el movimiento.
Fuente:
elaboración propia. |
– Fase postictal.
Comienza inmediatamente después de que la convulsión en el EEG haya terminado,
produciéndose un aumento tanto en
amplitud como en frecuencia y, por tanto, una
aproximación a la línea basal preanestésica.
2.
Electroencefalograma interictal
La TEC da lugar a
cambios globales y topográficos en la actividad funcional
cerebral. Durante el período postictal se produce un
considerable aumento de la actividad de onda lenta (delta y theta)
que refleja la extensión espacial de las poblaciones
neuronales sujetas a inhibición42,43. Es por ello que el EEG interictal
tiende a hacerse más lento y de mayor amplitud con la
administración de sucesivas sesiones de TEC, volviendo a la
normalidad de 1 a 12 meses tras la finalización del tratamiento. La
acetilcolina está involucrada en el desarrollo de estos
cambios electroencefalográficos, que son un signo de que
se han producido las convulsiones y de la persistencia de
los efectos de las mismas44,45.
Sackeim y sus
colaboradores (1996)32 en un estudio randomizado para diferentes
condiciones de aplicación de TEC a 62 pacientes con
trastorno depresivo mayor, concluyen que la inducción de
actividad de onda lenta en la corteza, está asociada a la
eficacia de la TEC. Enfatizan en el gradiente anteroposterior y en
el hecho que, tanto la reducción del FSC en la corteza
prefrontal como el aumento de la actividad delta, se relacionan
con la eficacia clínica.
Existen otros
hallazgos importantes descritos por diferentes grupos de
investigación7,9,46: la supresión postictal es más profunda con la TEC bilateral
que con la unilateral; las convulsiones con TEC bilateral
tienen mayor amplitud EEG ictal, simetría, coherencia,
regularidad morfológica y supresión postictal que con la TEC
unilateral; el aumento de la dosis eléctrica y el emplazamiento
bilateral de los electrodos correlacionan ambos positivamente con
mayor voltaje y regularidad del EEG ictal, y la mayor supresión
postictal de la actividad EEG se asocia a un desenlace del
tratamiento más positivo.
Mecanismos de la finalización de la
convulsión
Los mecanismos
implicados en la finalización de las crisis convulsivas han sido
descritos en base a estudios sobre epilepsia y en animales de
experimentación. Los de mayor relevancia implican los canales
de potasio, el cinc y el sistema gabaérgico.
– Canales de potasio
dependientes de ATP (KATP). Se expresan a nivel pre y
postsináptico en muchas regiones cerebrales. Su función está
controlada por el estado metabólico de la neurona. Un
descenso en la relación ATP: ADP activa estos canales,
limitando la excitabilidad celular y la liberación de
transmisores durante las fases de estrés metabólico. Estudios recientes
ponen de manifiesto la importancia de los KATP en el
control de la excitabilidad neuronal, la
propagación de la convulsión y el control del umbral convulsivo47.
– Canales de potasio
activados por proteínas G. Su activación representa un
importante mecanismo a través del que los
neurotransmisores y los neuropéptidos regulan la excitabilidad
neuronal. Se localizan a nivel pre y postsináptico y su activación
reduce la liberación de transmisores y la respuesta a los
input sinápticos47.
– Ácido gamma-aminobutírico
(GABA). Es el principal neurotransmisor
inhibitorio cerebral. Debido a que múltiples
experimentos han demostrado que las sustancias bloqueadoras de la
neurotransmisión gabaérgica generan convulsiones
en tejidos de control y a que diversos
potenciadores del sistema gabaérgico tienen acciones
antiepilépticas en pacientes humanos, se ha sugerido que la
actividad gabaérgica evita las convulsiones. Del mismo modo,
también se ha podido observar ampliamente que la
activación de las sinapsis glutamatérgicas generan
convulsiones48,49. Se postula que el estado
hipometabólico neural que sigue a la TEC se asocia y quizás está
producido por un aumento en la transmisión
gabaérgica26.
– Cinc. Se concentra
en determinadas vías excitadoras del SNC, especialmente en
las fibras musgosas del hipocampo, donde se ha sugerido
que modula la transmisión y la plasticidad
sináptica. Bancila y sus colaboradores (2004), utilizando
sinaptosomas de fibras musgosas de rata, aplicaron cinc en
concentraciones microsomales durante un episodio breve
anóxico-hipoglucémico. Hallaron que, a través de la
activación de los canales KATP presinápticos, el cinc protege las
neuronas frente a la hiperexcitación, la liberación excesiva
de transmisores y la excitotoxicidad. Postulan que el cinc
probablemente actúa como un neuroprotector endógeno en
condiciones patológicas como la epilepsia o la
apoplejía50.
Cambios en la
plasticidad sináptica y potenciación a largo plazo
En los últimos años,
muchas investigaciones sobre la neurobiología de la
memoria se han centrado en un fenómeno electrofisiológico
conocido como potenciación a largo plazo (PLP). Se trata
de una forma experimentalmente inducida de
plasticidad sináptica, fácilmente demostrable en el hipocampo, que
constituye un aumento duradero de la fuerza sináptica
excitatoria. Se ha propuesto como un mecanismo plausible en el
sustrato neuronal del aprendizaje. Diversos experimentos
han demostrado que la aplicación repetida de estimulación
electroconvulsiva en ratas, produce un marcado bloqueo de
la PLP en el hipocampo y en la neocorteza51,52. Este mecanismo ha
sido propuesto como posible causante de las
afectaciones cognitivas y amnésicas que aparecen tras un
ciclo de TEC53.
Por otro lado, se
postula que el efecto beneficioso de la TEC en el tratamiento
de los trastornos depresivos agudos54, puede estar
relacionado con cambios en la plasticidad sináptica y bloqueo de los
procesos de depresión a largo plazo a nivel estriatal55.
DISCUSIÓN Y
CONCLUSIONES
Existen diversos
aspectos que limitan la validez empírica de los mecanismos de
acción electrofisiológicos, tanto a nivel teórico como
metodológico. El aumento sustancial del umbral convulsivo es
una condición necesaria pero no suficiente para la respuesta a
la TEC. Los pacientes en que la fisiopatología de su trastorno no
esté relacionada con la excesiva desinhibición o
excitación podrían no responder al tratamiento9. Como ya
hemos visto, a lo largo del curso de tratamiento se
producen toda una serie de cambios dinámicos. El efecto
anticonvulsivo acumulado podría afectar de forma directa a la
expresión de la convulsión, independientemente de los efectos
producidos por la intensidad del estímulo eléctrico7.
Tras la revisión de
la literatura acerca de los mecanismos de acción
electrofisiológicos de la terapia electroconvulsiva podemos extraer las
siguientes conclusiones generales: 1) existen datos que
apoyan cambios electrofisiológicos, pero las diferentes
teorías neurobiológicas no pueden ser contempladas de forma
independiente debido a la complejidad de la función
cerebral que implica la interacción de los sistemas bioquímico, hormonal
y electrofisiológico; 2) la TEC posee propiedades
anticonvulsivantes, siendo la terminación de la crisis un
proceso inhibitorio activo esencial para su eficacia,
propiciando toda una serie de mecanismos a nivel neuronal; 3) el
umbral convulsivo es un filtro para muchos de los efectos
neurobiológicos del estímulo eléctrico y sólo después de que
haya sido rebasado existen relaciones consistentes entre la
dosis eléctrica y los efectos conductuales9; 4) se postula que el
bloqueo de la PLP que aparece tras la estimulación
electroconvulsiva puede ser el mecanismo subyacente a las
alteraciones cognitivas y amnésicas que aparecen con la
aplicación de la TEC; 5) la multitud de hallazgos publicados
sobre la TEC y estimulación electroconvulsiva, deben ser replicados
para conseguir diferenciar los efectos primarios
de aquellos que son secundarios y discernir cuales son realmente
terapéuticos; 6) se requieren más experimentos que
aumenten o bloqueen las propiedades anticonvulsivas de la
TEC y determinen los efectos que se producen en su
eficacia7; 7) el mayor conocimiento de los mecanismos de acción
puede permitir el desarrollo de otras técnicas más eficaces
basadas en los mismos.
Ver Bibliografía en el enlace.